Los secretos de la fenolftaleína
Objetivo: Ver cómo un indicador puede tener diferentes cambios de color

-
Material de laboratorio
Vasos
Pipetas
Tubos de ensayo
Gradilla para tubos de ensayo
-
Reactivos
Fenolftaleína (solución preparada: 0,1 g en 60 mL de etanol y 40 mL de agua)
Hidróxido sódico (NaOH)
Ácido clorhídrico 2 M (HCl)
Agua
-
Seguridad
¡¡¡No olvides los guantes, la bata de laboratorio y las gafas protectoras!!!
-
Preguntas
¿Cómo se prepara la solución de hidróxido sódico?
¿Qué se observa en el tercer tubo? ¿Por qué?
Procedimiento
- Prepara 100 mL de una solución 0,5 M de hidróxido sódico.
- Añade unas gotas de solución de fenolftaleína a la solución de hidróxido sódico hasta que se observe un color rosa intenso. A continuación, llena tres tubos de ensayo hasta la mitad con esta solución.
- En el primer tubo de ensayo, déjalo como control.
- En el segundo tubo de ensayo, añade la solución de ácido clorhídrico gota a gota hasta que desaparezca el color rosa.
- En el tercer tubo de ensayo, añade 2-3 trozos pequeños de hidróxido de sodio sólido y agita la solución para disolverlos. Observa lo que ocurre.
Explicación teórica
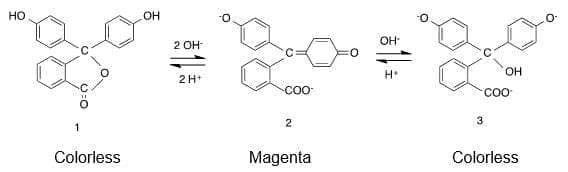
El comportamiento «normal» de la fenolftaleína es mostrar un color rosado en soluciones básicas y ser incolora en soluciones ácidas. Sin embargo, la fenolftaleína también puede volverse incolora en soluciones básicas más concentradas.
En solución ácida, la fenolftaleína adopta la forma 1, que es incolora. Con la adición de hidróxido sódico, se pierden dos protones para producir el dianión 2, de color rojo, mientras que una adición básica adicional da lugar a la forma 3, que también es incolora.


Creemos un futuro más brillante
Únete a nuestro equipo para trabajar con investigadores de renombre, emprender proyectos innovadores y contribuir a avances científicos significativos.
Únete a nosotros!













