Àcid cítric en sucs
Objectiu: Determinar l’àcid cítric en suc de taronja acabat de preparar i en suc comercial (també es pot realitzar amb suc de llimona)

-
Materials de laboratori
Erlenmeyer
Vases de precipitats
Bureta
Espremedora de fruites
-
Reactius
Taronges
Llimones
Suc de taronja/llimona disponible al comerç
Fenolftaleïna
Hidròxid de sodi 0,5 M (NaOH)
Aigua
-
Seguretat
No oblideu els guants, la bata de laboratori i les ulleres de seguretat!!!
-
Preguntes
Quina reacció té lloc durant la valoració?
Determineu la concentració d'àcid cítric en tots els sucs. A quines conclusions es pot arribar?
Procediment
- Espremeu la taronja i la llimona i emmagatzemeu els sucs en dos gots.
- Afegiu 10 ml de suc de taronja en un matràs Erlenmeyer i després afegiu 25 ml d’aigua i unes gotes de fenolftaleïna.
- Titular aquesta solució amb hidròxid de sodi 0,5 M.
- Repetiu el procés amb 10 ml de suc de llimona acabat de preparar.
- Finalment, repetiu el procés amb els sucs comercials i compareu els resultats.
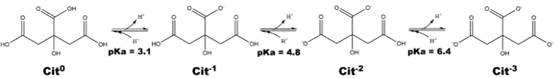
Explicació teòrica
És ben conegut que els sucs de taronja i llimona són àcids. El principal compost químic responsable d’aquesta acidesa és l’àcid cítric, un triàcid carboxílic que es produeix per la fermentació dels sucres (> 106 tones anuals) per al seu ús en begudes i aliments (70%), detergents (20%) i cosmètics, productes farmacèutics i altres aplicacions (10%).
En contacte amb l’aigua, la desprotonació dels tres àcids carboxílics dóna lloc a tres equilibris àcid/base, cadascun amb la seva constant d’acidesa (Ka):
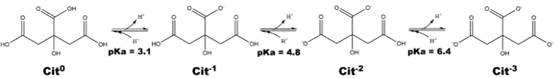
Quan es valora l’àcid cítric amb NaOH, el pH de la solució es torna més bàsic i els àcids es desprotonen. Un cop hem afegit la base suficient per desprotonar tots els àcids (formant Cit3- en el diagrama), la següent gota de NaOH fa que el pH de la solució que s’està titulant augmenti bruscament de 7 a més de 9. Aquest canvi de pH fa que la fenolftaleïna es torni rosa, ja que el seu pH final està al voltant de 8-8,5. En aquest punt, la valoració es considera completa.
Com que coneixem el volum de NaOH 0,5 M que hem utilitzat, podem calcular els mols de base necessaris per neutralitzar l’àcid cítric present en el suc. Sabent que la relació estequiomètrica entre el triàcid i la base és 1:3, podem calcular els mols d’àcid cítric presents a la mostra. Finalment, podem utilitzar el pes molecular de l’àcid cítric (192,124 g/mol) per calcular la massa.
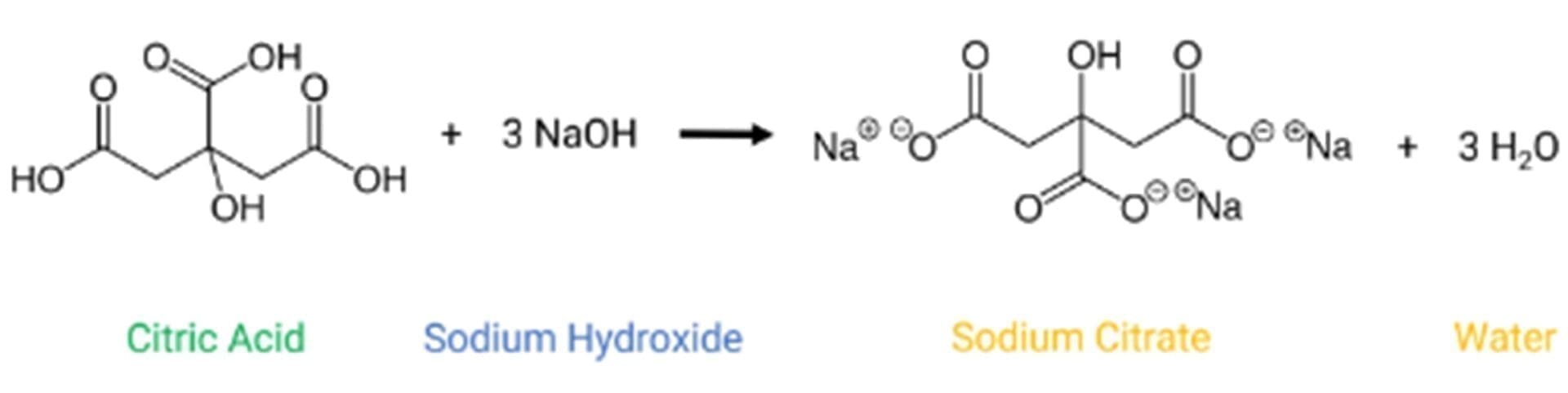
La reacció química és:

Creem un futur més brillant
Uneix-te al nostre equip per treballar amb investigadors reconeguts i fer front a les novetats
projectes i contribuir a avenços científics significatius














